nanopartículas de oro Se refiere a partículas de oro ultrafinas con un tamaño de entre 1 y 100 nanómetros. A diferencia del oro macroscópico, el oro a nanoescala presenta importantes efectos de resonancia de plasmones superficiales (SPR), efectos de tamaño cuántico y una enorme superficie específica. Estas características le confieren excelentes propiedades ópticas, eléctricas y catalíticas en entornos biológicos complejos. Además, las nanopartículas de oro se han convertido en un importante nexo entre la nanotecnología y la medicina clínica debido a sus propiedades químicas estables y su baja toxicidad biológica.
1. Aplicación en el diagnóstico médico
1.1 Biosensado y detección rápida
Una de las aplicaciones más extendidas de las nanopartículas de oro es como marcadores para diagnósticos in vitro (DIV). El caso más típico es el inmunoensayo de flujo lateral (como las pruebas de embarazo tempranas y las pruebas rápidas de detección de COVID-19), que utiliza la fuerte absorbancia y el cambio de color del nanopulvo de oro para lograr la detección de la señal visible a simple vista.
1.2 Mejora del contraste en imágenes
El elevado número atómico del oro le confiere una excelente capacidad de atenuación de rayos X. En comparación con los agentes de contraste de yodo tradicionales, las nanopartículas de oro, utilizadas como agentes de contraste para tomografía computarizada (TC), presentan un mayor tiempo de circulación sanguínea y menor toxicidad renal. Asimismo, sus propiedades fototérmicas le permiten desempeñar un papel fundamental en la imagen fotoacústica (PAI), mejorando significativamente el contraste de imagen del tejido tumoral.
2. Aplicaciones innovadoras en el campo del tratamiento
2.1 Terapia fototérmica (PTT)
Las nanopartículas de oro pueden convertir eficientemente la energía lumínica en energía térmica bajo irradiación de luz infrarroja cercana. Mediante la modificación de su superficie (por ejemplo, mediante la unión de folato o anticuerpos), estas nanopartículas pueden agregarse con precisión en el sitio del tumor. Tras la irradiación láser, la alta temperatura generada localmente es suficiente para destruir las células cancerosas, causando un daño mínimo a los tejidos sanos circundantes.
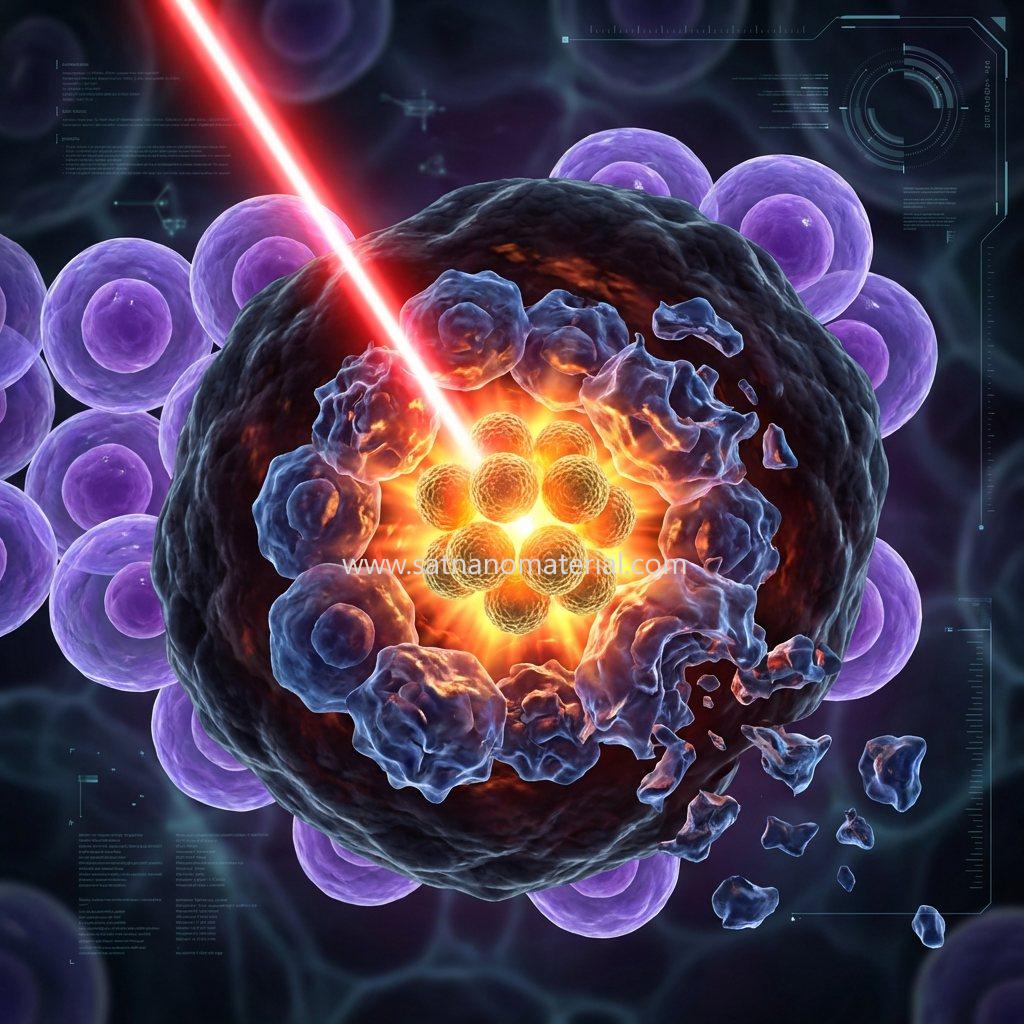
2.2 Sensibilización a la radioterapia
Dado que las nanopartículas de oro pueden absorber rayos de alta energía y liberar electrones secundarios (fotoelectrones y electrones Auger), el uso de nanopartículas de oro durante la radioterapia puede aumentar significativamente la dosis de radiación local, mejorando así la tasa de eliminación de células tumorales y reduciendo el riesgo de exposición para los tejidos normales.
2.3 Administración dirigida de fármacos
La enorme superficie específica del nanopulvo de oro permite cargar una gran cantidad de fármacos quimioterapéuticos, proteínas o ácidos nucleicos (ADN/ARN). Aprovechando su química de tioles superficiales (enlaces Au-S), los científicos pueden injertar fácilmente ligandos en la superficie de las nanopartículas, logrando una administración precisa y una liberación controlada del fármaco, lo que reduce los efectos secundarios tóxicos sistémicos.
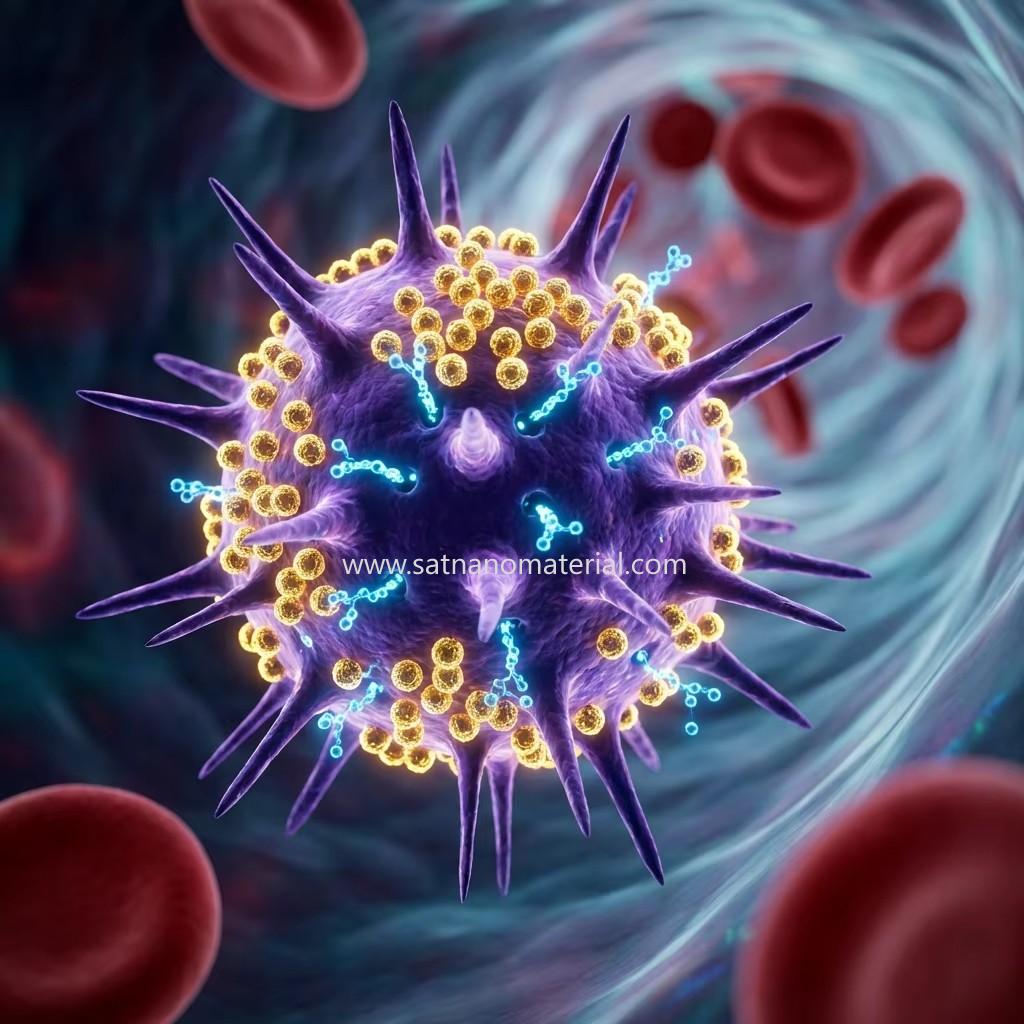
Los distintos tamaños de nanopartículas de oro tendrán diferentes aplicaciones. A continuación se presentan los datos de los parámetros recopilados por Gary, un técnico de la empresa SAT NANO.
3. Diámetro/Tamaño: Este es el parámetro fundamental que afecta al rendimiento de las nanopartículas de oro.
3.1 Menos de 20 nm: se utilizan principalmente para la administración de fármacos y la eliminación renal. Por ejemplo, el diámetro de las partículas utilizadas para la administración de fármacos suele ser de entre 13 y 18 nm, mientras que las partículas utilizadas para la focalización hepática pueden controlarse entre 10 y 30 nm. Los nanoclústeres de oro ultrapequeños (como Au₂₅) están compuestos por 25 átomos de oro y suelen tener un diámetro inferior a 3 nm.
3.2 20-50 nm: Ampliamente utilizado en imágenes ópticas y terapia fototérmica, como partículas de 3,19 nm para imágenes y nanobarras de oro de 25 × 47 nm utilizadas en terapia fototérmica.
3.3 50-200 nm: Se utilizan comúnmente en escenarios que requieren una alta eficiencia de conversión fototérmica, como las nanoestructuras de oro multicapa (<100 nm) empleadas en la terapia fototérmica de tumores y las sondas de nanooro utilizadas para la detección inmunohistoquímica. Los estudios han demostrado que las partículas esféricas más grandes (aproximadamente 102 nm) son absorbidas con mayor facilidad por ciertas células.

4. Propiedades ópticas: Esta es la base para que las nanopartículas de oro se utilicen en diagnóstico por imagen y terapia.
4.1 Pico de absorción característico (λ máx): Las nanopartículas de oro esféricas suelen presentar un pico de absorción alrededor de 520-530 nm, mientras que las nanobarras de oro tienen dos picos de absorción por resonancia plasmónica: uno horizontal y otro vertical. El pico vertical puede desplazarse hacia la región del infrarrojo cercano (generalmente 600-900 nm) ajustando la relación de aspecto de la nanobarra. La energía lumínica en esta banda penetra en tejidos más profundos, lo que la hace muy adecuada para la terapia fototérmica y la obtención de imágenes de tejidos profundos.
4.2 Características de luminiscencia: Cuando se utiliza para imágenes biológicas, un alto rendimiento cuántico (como el 12,9 %) significa señales más brillantes, mientras que una vida útil de luminiscencia ultralarga (alrededor de 1 microsegundo) se puede proteger eficazmente de la fluorescencia de fondo de los tejidos biológicos mediante la tecnología de compuerta temporal, lo que da como resultado imágenes de mayor resolución.
4.3 Modificación de la superficie: Para aumentar la estabilidad, la biocompatibilidad y la especificidad, la superficie de las nanopartículas de oro generalmente necesita ser "disfrazada".
4.4 Modificación con PEG: El polietilenglicol (PEG) es la molécula modificadora más utilizada, que actúa como una "capa de invisibilidad" para las partículas, reduciendo su eliminación por el sistema inmunitario y prolongando su tiempo de circulación en el organismo. Por ejemplo, el PEG3000 modificó partículas de oro de 40 nm.
4.5 Modificación molecular dirigida: Al unir ligandos específicos, las nanopartículas pueden encontrar con precisión sus objetivos. Por ejemplo, la modificación con GalNAc (N-acetilglucosamina) permite dirigir la acción a la diana hepática; la unión de anticuerpos puede utilizarse para la obtención de imágenes y el tratamiento dirigido de tumores.
En definitiva, la elección de los parámetros para las nanopartículas de oro depende totalmente de los objetivos específicos de su aplicación:
Si el objetivo es obtener imágenes biológicas de alta resolución, especialmente imágenes de tejidos profundos, la atención puede centrarse en partículas con un tamaño de unos pocos nanómetros, un alto rendimiento cuántico y características de luminiscencia en el infrarrojo cercano.
Si el objetivo es la terapia fototérmica para tumores, es necesario elegir partículas con una fuerte absorción en la región del infrarrojo cercano (como 808 nm) y una alta eficiencia de conversión fototérmica (como el 77%), y su tamaño óptimo suele ser inferior a 100 nm.
Si el objetivo es construir un sistema de administración de fármacos dirigido, las partículas con un tamaño de 10 a 30 nm y una superficie fácil de modificar con múltiples funciones (como la unión de PEG y ligandos de direccionamiento) son una opción más adecuada.
SAT NANO es un proveedor de los mejores nanopartículas de oro En China, podemos ofrecer nanopartículas de 20-30 nm. Si necesita dispersión de oro, también podemos suministrarla. Si tiene alguna consulta, no dude en contactarnos a través de admin@satnano.com.
 Servicio en línea
Servicio en línea 13929258449
13929258449 admin@satnano.com
admin@satnano.com + 8613929258449
+ 8613929258449