¿Por qué se agregan las nanopartículas?
1. Mecanismo impulsado por energía libre de superficie
Las nanopartículas tienen una mayor área superficial específica y átomos superficiales insaturados, lo que aumenta la energía libre superficial. El contacto entre múltiples partículas puede reducir el área superficial total, liberar energía interfacial y, por lo tanto, disminuir la energía libre del sistema. Esta tendencia a la minimización de la energía es la fuerza termodinámica intrínseca que impulsa la aglomeración espontánea de partículas y es una fuente común de aglomeración a escala nanométrica.
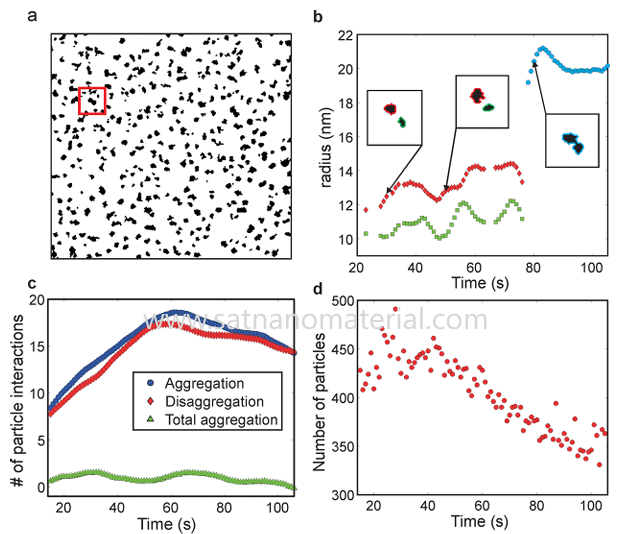
2. Electricidad estática e inestabilidad eléctrica de doble capa.
La doble capa eléctrica formada por partículas cargadas puede proporcionar un estado de dispersión estable de repulsión electrostática. Cuando el pH se aproxima al punto isoeléctrico o la fuerza iónica aumenta, la bicapa se comprime, la fuerza repulsiva disminuye y la energía potencial de atracción entre partículas predomina, lo que provoca la aglomeración. La estabilidad de esta barrera potencial determina la capacidad antiagregante del sistema.
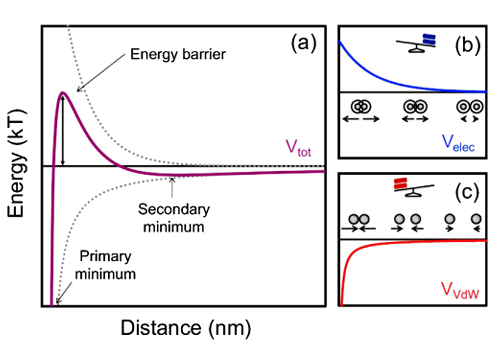
3. La influencia de la acción del medio disolvente
Las partículas en solución dependen de la capa de solvatación para lograr la estabilidad de la interfaz. Si el disolvente tiene baja polaridad y baja afinidad, es difícil formar una capa de solvatación efectiva, lo que aumenta el contacto directo entre partículas, intensifica las fuerzas de van der Waals y desencadena la aglomeración. Por lo tanto, las propiedades físicas y químicas de los disolventes afectan directamente el estado de dispersión de las partículas.
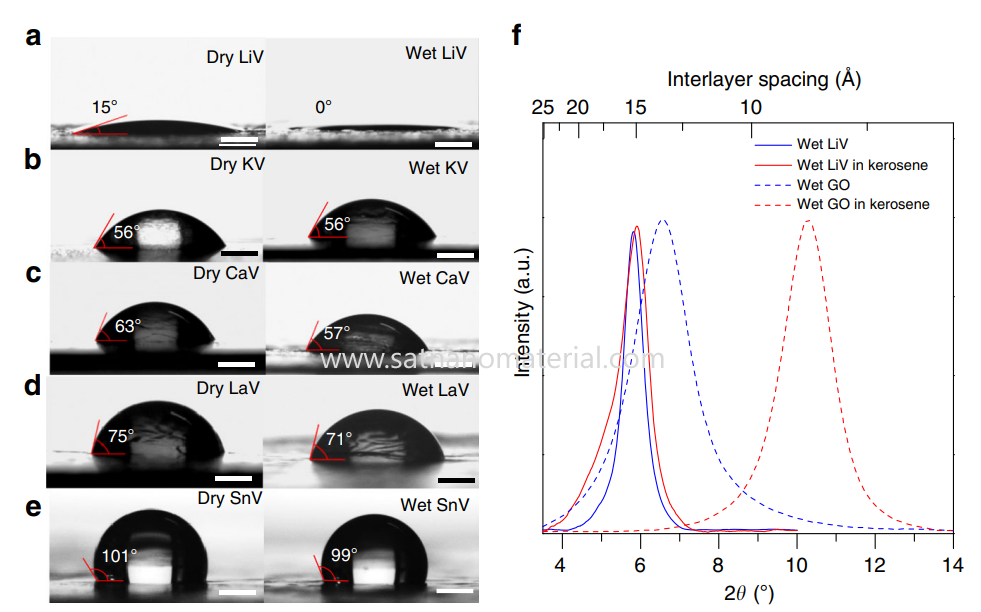
4.Modo de agregación de la unión química
Las partículas con alta reactividad pueden formar agrupaciones estables mediante enlaces de hidrógeno, coordinación o enlaces covalentes de grupos funcionales como los grupos hidroxilo y carboxilo en sus superficies. Este enlace químico hace que la agregación sea irreversible y difícil de disociar físicamente. Este proceso se basa en la reactividad química de los estados de energía superficial y los grupos funcionales.
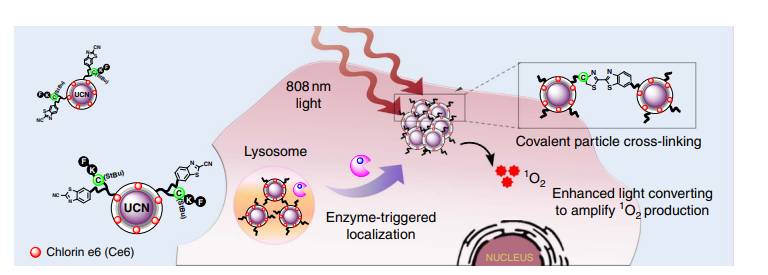
¿Por qué se dispersan las nanopartículas?
1. Establecer una barrera de energía potencial mediante repulsión electrostática.
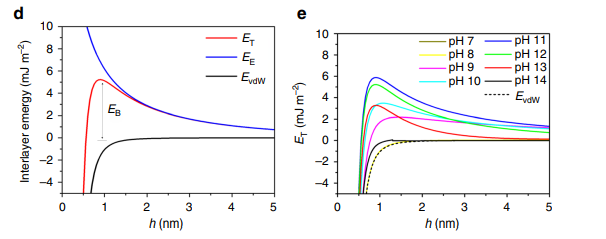
La carga superficial de las partículas formará una estructura de doble capa eléctrica en el líquido, y cuando dos partículas se aproximan, se genera repulsión electrostática entre las capas. Este efecto repulsivo puede crear una barrera de energía potencial entre las partículas, suprimiendo eficazmente la agregación causada por la atracción de corto alcance. Si existe una barrera de potencial suficientemente alta en la energía potencial total del sistema, las partículas se encuentran en un estado dinámicamente estable. Este mecanismo se basa en la densidad de carga, la constante dieléctrica y la fuerza iónica, y es una base estable común para los coloides acuosos.
2. Intervalo de mejora del efecto de impedimento estérico espacial
El efecto de impedimento estérico se genera por la adsorción o injerto de segmentos de polímero en la superficie de las partículas. Cuando las partículas tienden a aproximarse, estas estructuras moleculares generan fuerzas de compresión y repulsión conformacionales, impidiendo el contacto entre ellas.
Este mecanismo no depende de la carga superficial y es adecuado para sistemas apolares o de alta fuerza iónica. El impedimento espacial proporciona una barrera física y es uno de los mecanismos de dispersión más comunes en sistemas recubiertos con polímeros o surfactantes, particularmente evidente en partículas con superficie modificada.

3. La capa de solvatación impide el contacto.
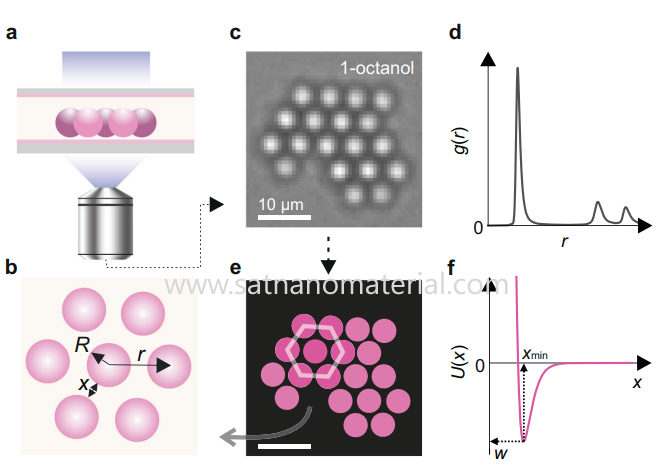
Cuando las partículas forman una capa de solvatación estable con las moléculas de disolvente, esta capa proporciona importantes barreras energéticas cuando las partículas se aproximan, impidiendo el contacto directo entre ellas. El espesor y la estabilidad de la capa de solvatación dependen de la polaridad, la capacidad de enlace de hidrógeno y la afinidad con la superficie de la partícula del disolvente. Si el contacto entre partículas necesita superar la energía de desorción de la capa de solvatación, esta barrera energética puede reducir eficazmente la probabilidad de aglomeración y constituye un importante mecanismo de garantía de dispersión en condiciones de repulsión no eléctrica.
4.La funcionalización de la superficie mejora la estabilidad química.
La funcionalización de superficies puede introducir carga, estructura espacial o factores reguladores hidrofóbicos para mejorar la repulsión de partículas o la compatibilidad interfacial, mejorando así la estabilidad de la dispersión. Mediante el injerto de ligandos, cadenas poliméricas o grupos funcionales, la superficie puede lograr un doble mecanismo de repulsión eléctrica y protección espacial, lo que dificulta la aproximación de partículas y la formación de agregados. Este método se utiliza ampliamente en sistemas como óxidos metálicos y puntos cuánticos, y es una de las estrategias clave para lograr una dispersión controlable.
SAT NANO es el mejor proveedor de nanopolvo y micropolvo en China, podemos suministrar polvo metálico , polvo de aleación , polvo de óxido y polvo de carburo Si tiene alguna consulta, no dude en contactarnos en admin@satnano.com
 Servicio en línea
Servicio en línea 13929258449
13929258449 admin@satnano.com
admin@satnano.com + 8613929258449
+ 8613929258449